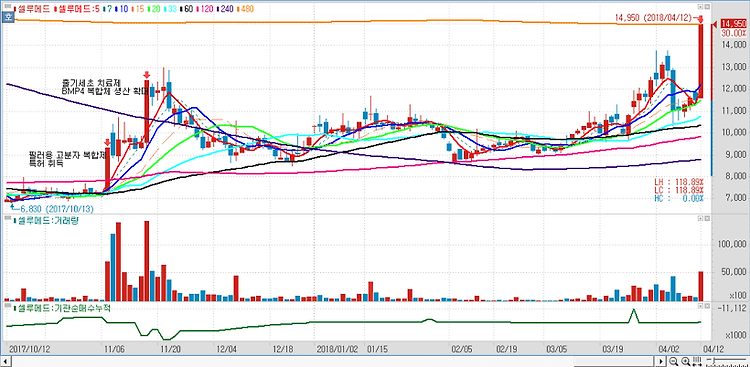
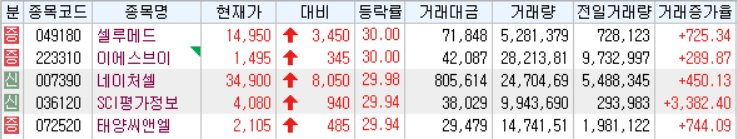
셀루메드(049180)가 골이식재 해외 수출 확대 기대감에 급등하며 상한가를 나타내고 있다. 골이식재 사업에 대한 기대가 매수세로 반영되는 양상이다. 회사는 이날 골이식재인 라퓨겐 DBM(Rafugen DBM)이 미국 식품의약국(FDA)의 승인을 받았다고 공시했다. 이를 통해 전세계 근골격계 시장 진출의 교두보를 확보했다고 회사측은 전했다. ----------------------------------------------------------------------------------------------------------------------"블루오션스탁"에서 제공하는 모든 정보는 투자판단의 참고자료이며, 투자판단의 최종 책임은 이용자에게 있습니다.