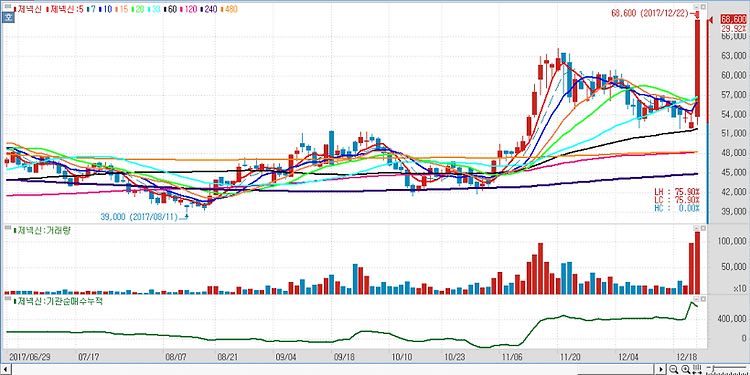
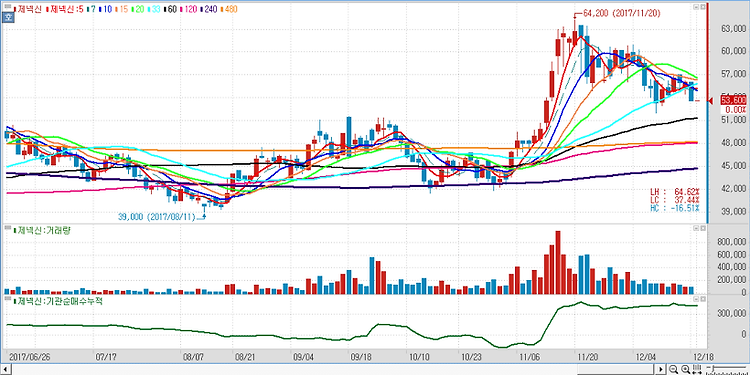
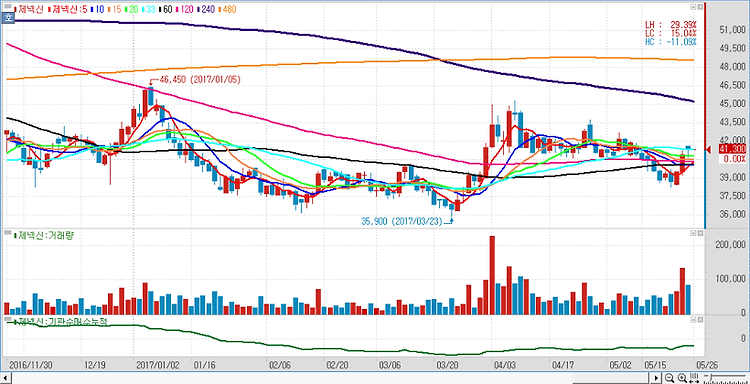
제넥신(095700)에 대해 2500억원의 자금 조달로 항암제인 하이루킨의 다양한 병용투여 임상이 가능해져 비상할 준비를 마쳤다고 진단했다. 제넥신은 전날 유상증자와 전환사채(CB) 발행으로 2500억원의 자금을 조달하는 내용을 공시했다. 조달된 자금으로 주요 파이프라인 임상 및 연구개발에 약 1900억원, 제넥신의 자회사인 NIT의 지분 인수와 R&D(연구개발) 목적 투자를 위해 600억원이 집행될 예정이다. 제넥신의 이번 자금조달은 결국 하이루킨의 원활한 임상 수행과 다수 파이프라인의 연구개발을 위한 것이며 제넥신은 지난 20일 하이루킨의 뇌암 환자 대상 임상시험이 미 FDA로부터 승인을 받았다. 약 50~70명의 뇌암 환자를 대상으로 안전성과 효능을 평가하는 1상과 소규모 2상으로 구성되며 항암 환..