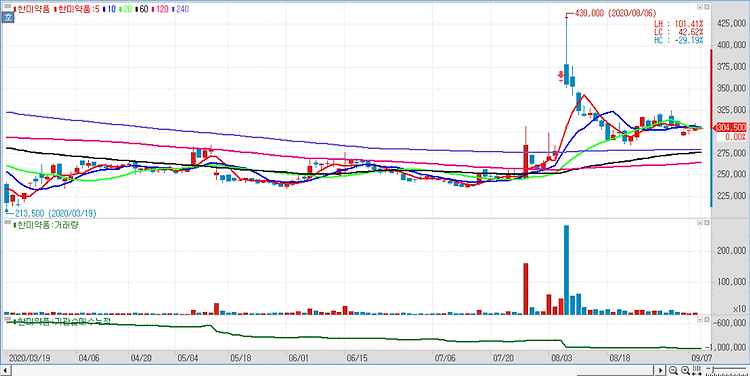
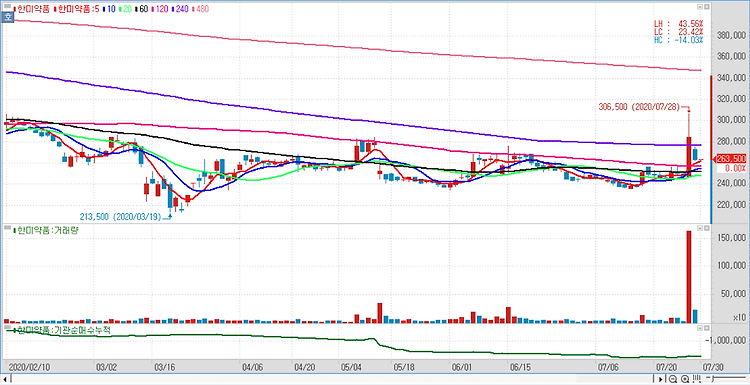
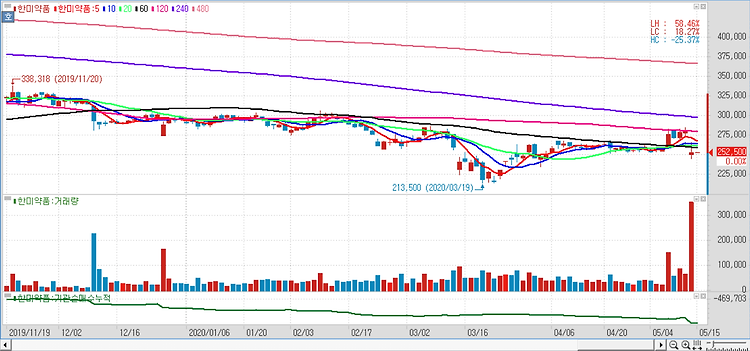
한미약품(128940)은 사노피가 ‘에페글레나타이드’의 당뇨치료제 임상 개발을 중단하기로 확정했다고 밝혔다. 이에 따라 한미약품은 당뇨치료제가 아닌 다른 적응증 탐색 및 병용요법 연구, 새로운 파트너링 체결 등 새로운 기회를 모색한다는 방침이다. 사노피는 지난 5월 에페글레나타이드 반환 의사를 한미약품에 통보한데 이어 8일 이를 확정하고 각 임상 사이트에 통지했다. 에페글레나타이드 임상 3상은 30여 개국 300여 개 임상센터에서 6,000여 명 환자를 대상으로 진행돼왔다. 사노피의 주요 사업전략 변경에 따른 개발 중단 결정과 더불어, 세계적 코로나19 팬데믹으로 각국 의료체계가 흔들려 수천 명 대상 동시다발적 임상을 기한 내 진행할 수 없다는 현실적 어려움 또한 이번 최종 결론에 영향을 미쳤다. 에페글..